动物实验
肿瘤相关动物实验综合解决方案
- 乳腺癌动物实验综合解决方案
- 前列腺癌动物实验综合解决方案
- 卵巢癌动物实验综合解决方案
- 子宫内膜癌动物实验综合解决方案
- 宫颈癌动物实验综合解决方案
- 小细胞肺癌动物实验综合解决方案
- 非小细胞肺癌动物实验综合解决方案
- 尤文肉瘤动物实验综合解决方案
- 白血病动物实验综合解决方案
- 结直肠癌动物实验综合解决方案
- 肝细胞癌动物实验综合解决方案
- 肾细胞癌动物实验综合解决方案
- 胃癌/胃食管结合部腺癌动物实验综合解决方案
- 胰腺导管腺癌动物实验综合解决方案
- 胶质母细胞瘤/高级别胶质瘤动物实验综合解决方案
- 膀胱癌/尿路上皮癌动物实验综合解决方案
- 软骨肉瘤动物实验综合解决方案
- 骨肉瘤动物实验综合解决方案
- 黑色素瘤动物实验综合解决方案
- 头颈鳞癌动物实验综合解决方案
- 口腔鳞癌动物实验综合解决方案
皮肤相关疾病动物实验综合解决方案
骨相关疾病动物实验综合解决方案
免疫系统相关疾病动物实验综合解决方案
泌尿系统疾病动物实验综合解决方案
呼吸系统疾病动物实验综合解决方案
神经系统与精神类疾病动物实验综合解决方案
- 脑缺血/脑血管病疾病动物实验综合解决方案
- 神经退行性疾病动物实验综合解决方案
- 抑郁症/情感障碍动物实验综合解决方案
- 焦虑障碍动物实验综合解决方案
- 心境障碍(双相/躁狂)动物实验综合解决方案
- 焦虑-创伤谱系动物实验综合解决方案
- 精神病性障碍疾病动物实验综合解决方案
- 癫痫动物实验综合解决方案
- 头痛与疼痛动物实验综合解决方案
- 疼痛动物实验综合解决方案
- 周围神经病变动物实验综合解决方案
- 脱髓鞘/自身免疫疾病动物实验综合解决方案
- 睡眠障碍动物实验综合解决方案
- 围手术期脑功能障碍动物实验综合解决方案
- 谵妄/急性脑病动物实验综合解决方案
- 肿瘤相关神经损伤动物实验综合解决方案
- 创伤性神经系统损伤动物实验综合解决方案
内分泌代谢动物实验综合解决方案
生殖系统疾病动物实验综合解决方案
抗炎镇痛药效筛选实验综合解决方案
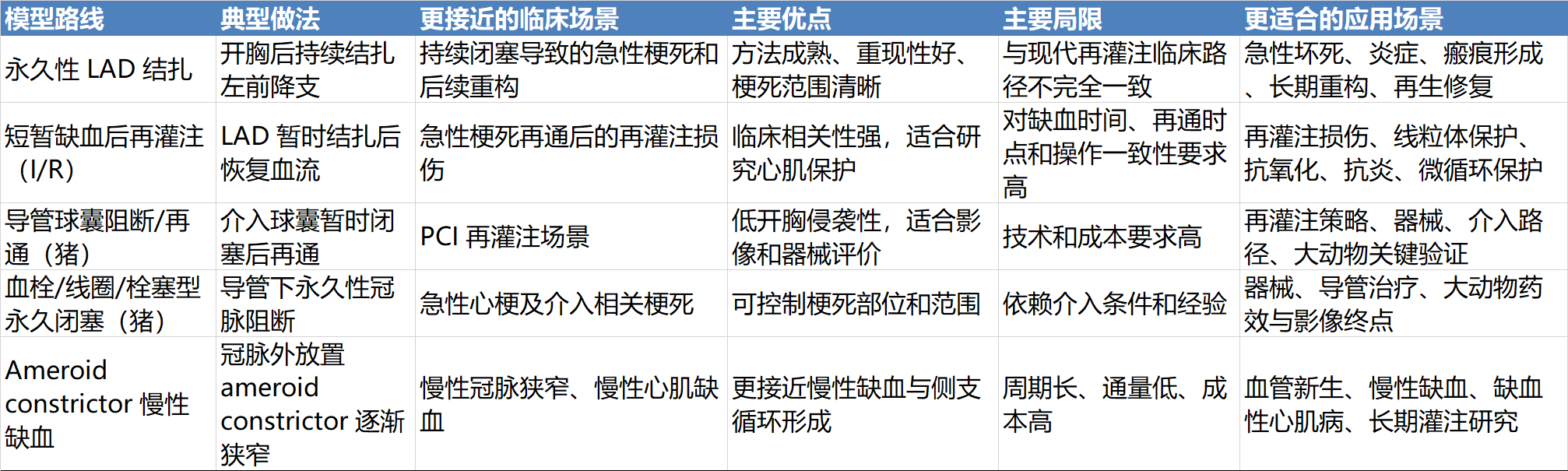
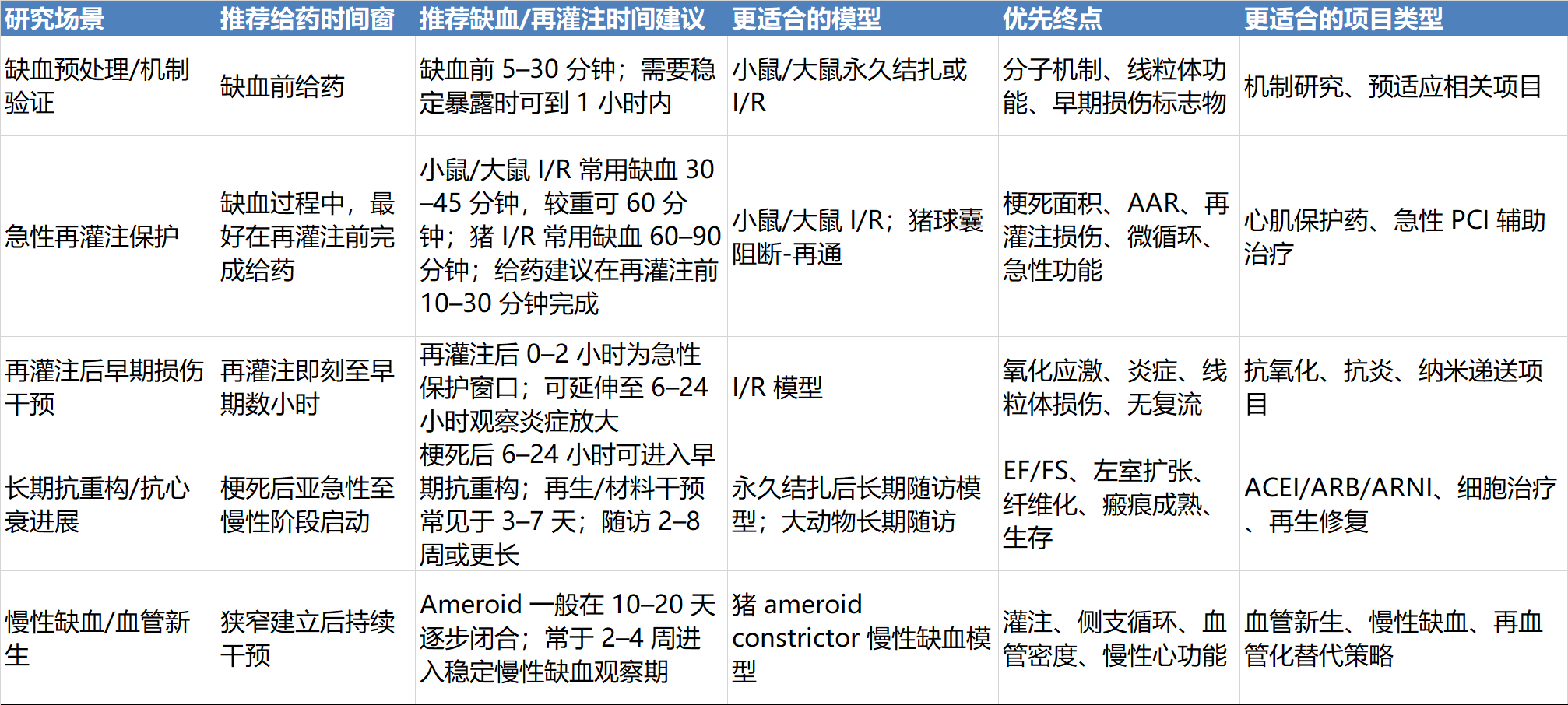
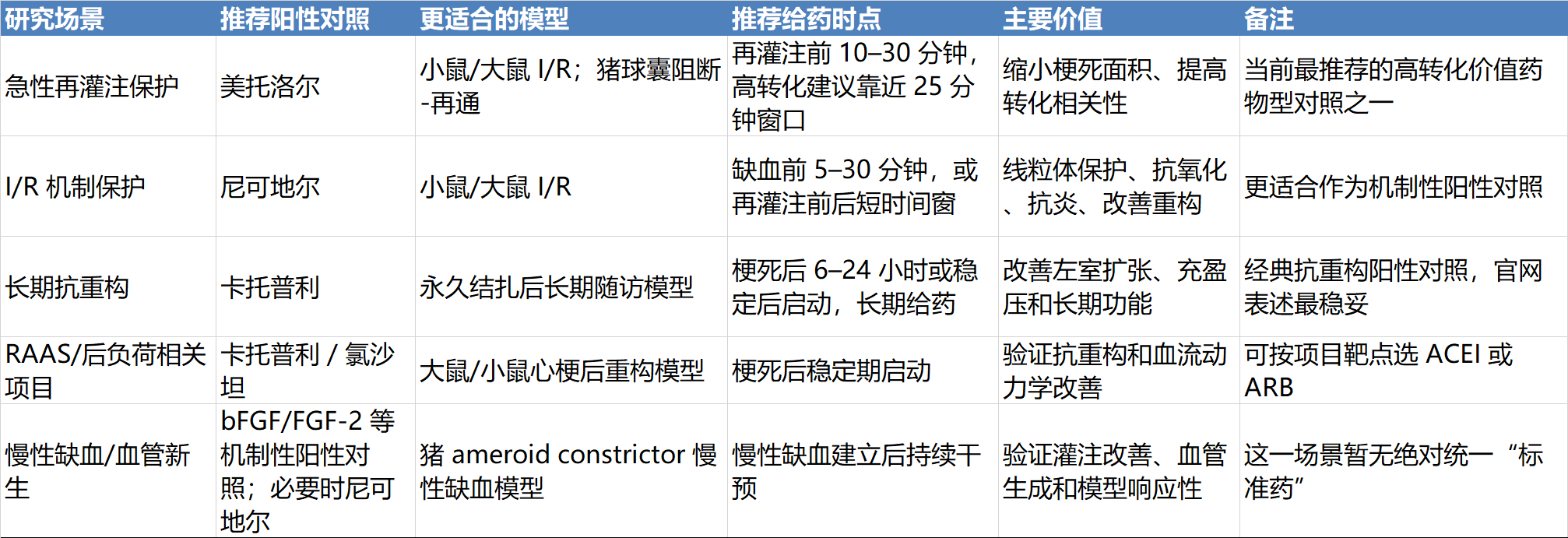
心血管系统动物实验综合解决方案
消化系统疾病动物实验综合解决方案
眼耳鼻喉相关疾病动物实验综合解决方案
血液系统疾病动物实验综合解决方案
中医症候动物实验综合解决方案
分子生物学实验
● 细胞实验整体解决方案
● 细胞层面药效筛选综合解决方案
● 分子机制实验整体解决方案
● 整体实验服务解决方案
● western blot实验服务
● 流式细胞术实验服务
● PCR 实验服务
● 细胞增殖检测综合解决方案
● 细胞表型谱系转化研究综合解决方案
● 自噬研究综合解决方案
● 免疫组化(IHC)实验服务
● 不同类型细胞死亡方式研究综合解决方案
● 肿瘤微环境研究综合解决方案
● 巨噬细胞极化研究综合解决方案
● 干细胞研究综合解决方案
● circRNA 研究综合解决方案
● lncRNA 研究综合解决方案
● 外泌体相关研究综合解决方案
● 代谢重编程研究综合解决方案
● T 细胞极化研究综合解决方案
● 树突细胞研究综合解决方案
● 细胞间通讯/交互研究综合解决方案
● 不同细胞应激方式研究综合解决方案
● 蛋白信号通路研究综合解决方案
● ELISA 实验服务
● 免疫共沉淀(co-IP)实验服务
● 免疫荧光(IF)实验服务
● 荧光素酶报告基因实验服务
● 原位杂交(ISH)实验服务
● 染色质免疫沉淀ChIP 实验服务
● RIP 实验服务
● 药代动力学实验服务(PK实验)
● EMSA实验服务
● RNA pull-down 实验服务
● 标签蛋白 Pull-down 实验服务
● DNA pull-down 实验服务
● Transwell 实验服务
● 细胞划痕实验服务
● 小动物活体成像实验服务
● 代谢组学
● 病理切片染色






 E-mail
E-mail